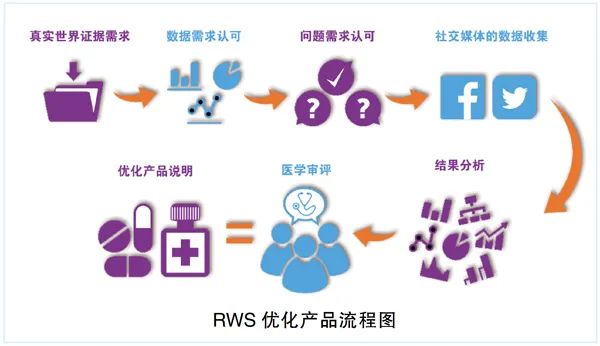
7月7日,國家藥品監(jiān)督管理局藥品審評中心(CDE)組織起草了《藥物真實世界研究設計與方案框架指導原則(征求意見稿)》,指導申辦者科學合理地設計真實世界研究,明確真實世界研究方案撰寫的技術要求(征求意見時限為自發(fā)布之日起2個月)。
關于真實世界研究(Real World Study,RWS)的理論性文章有很多,但到實際操作層面,往往存在許多問題。最常見的問題是將RWS與用于新藥注冊上市的研究相混淆。
坑點① 自訂方案太嚴格
對策:區(qū)分上市前后研究
RWS涵蓋的范圍很廣泛,有多種多樣的研究類型,包括回顧性研究、前瞻性研究等。但是很多前瞻性RWS方案設計模仿了用于新藥注冊申報研究的設計。
例如,設計了非常嚴格的入排標準、規(guī)定了很多與研究相關的實驗室檢查和特殊檢查、規(guī)定了嚴格的訪視窗口(不許超窗)、有嚴格的關于藥品使用的規(guī)定、有嚴格的隨機程序甚至伴有盲法設計、不良事件的收集采用與注冊研究同樣的方法等等。之所以存在這樣的問題,很大程度與方案設計人員對RWS的理解存在偏差有關。
對于RWS而言,有的研究是針對疾病而非藥品進行的,例如真實世界的注冊登記(Registry)研究;有的研究是針對上市后的藥品。應該注意上市后研究和上市前研究的區(qū)別。
用于新藥注冊的藥品上市前的研究,由于藥品的療效和安全性沒有得到驗證,需要有嚴格的程序來體現(xiàn)藥品的療效和安全性。雖然這些嚴格的設計和程序或多或少會對受試者的權益和安全性產(chǎn)生影響,但是為了新藥的審批和人類健康水平的提高,經(jīng)過藥監(jiān)部門和倫理委員會的審查,這種影響通常被認為是值得的(對個體和社會的益處大于風險, ICH E6 R2, 2.2)。
已經(jīng)上市的藥品研究其療效和安全性已經(jīng)得到了確認,若仍然要求受試者服從過于嚴格的設計和程序,或者對受試者的權益造成影響,從倫理的角度就不一定能夠被接受。
坑點② 試驗目的不確切
對策:遞交IND或更佳
有的研究的目的不是很明確。例如,增加已經(jīng)上市藥品的適應癥。須知,現(xiàn)今藥監(jiān)局對臨床研究的審批速度提升,早已不是以往需要排隊兩三年的情況。企業(yè)增加已經(jīng)上市藥品的適應癥完全可以通過正式遞交IND審批,做一個正規(guī)的Ⅲ期研究,這樣便不存在數(shù)據(jù)不被藥監(jiān)部門認可的問題。
有的研究的目的不太正確。例如,為了刺激銷售而開展,這樣目的導向下的研究一般無法產(chǎn)生積極的結(jié)果。
坑點③ 試驗管理非獨特
對策:提效率嚴數(shù)量要求
有一些項目管理人員將RWS的管理與新藥注冊申報研究的管理等同起來,這樣既浪費資源,也沒有效率。RWS的項目管理計劃、監(jiān)查計劃、質(zhì)量管理計劃、安全性管理計劃等都具有自身的特點,不能照搬新藥注冊申報的臨床研究。
RWS對于數(shù)據(jù)質(zhì)量的要求不像新藥注冊申報的研究,因為這個階段藥品的療效和安全性已經(jīng)得到了確認。但是,RWS需要納入更大的樣本量、有更多的中心數(shù)量、擁有更豐富的數(shù)據(jù)量等。每個監(jiān)查員管理的中心數(shù)量是新藥注冊研究的許多倍。RWS的監(jiān)查員更像是臨床研究管理員,因為這類研究一般不需要做原始資料核查,中心化的遠程監(jiān)查可以替代大部分現(xiàn)場監(jiān)查,而遠程監(jiān)查可以通過數(shù)據(jù)管理人員和醫(yī)學人員實施。
坑點④ 市場地位缺認可
對策:積累經(jīng)驗擁抱行業(yè)
一些監(jiān)查員或項目經(jīng)理有一個普遍的認識誤區(qū):做新藥注冊的研究最有含金量,做醫(yī)療器械的研究次之,而做RWS最沒有含金量。這種看法是不對的。
所有類型的研究都有各自的用處。就目前的人才市場情況來看,如果一個項目經(jīng)理對RWS的管理非常有經(jīng)驗,很多大數(shù)據(jù)公司都會高薪來搶人。監(jiān)查員也是如此,一個能夠同時管理幾十家中心并且對各家中心的人員、機構的要求、倫理委員會的程序非常熟悉,且具備迅速解決各種問題能力的監(jiān)查員,在市場上同樣熾手可熱。